|
Nanokatalyse til forbedret afsvovling af fossile brændstoffer
Katalysatorer bruges i stor skala til at accelerere og kontrollere tusindvis af vigtige kemiske reaktioner i den kemiske industri. De danner derved grundlaget for en produktion med en årlig omsætning på adskillige billioner kroner på verdensplan samt uundværlig miljøbeskyttelse, som vi fx kender det fra bilkatalysatoren.
En katalysator udmærker sig ved, at den kan accelerere en kemisk reaktion eller styre den i en given retning uden at katalysatoren selv bliver forbrugt i den kemiske proces, og man kan derved få kemiske reaktioner, der normalt ville tage årevis, til at forløbe på et splitsekund.
Selvom man industrielt har udnyttet katalytiske processer i op mod 100 år, mangler der i mange tilfælde en fyldestgørende mikroskopisk forståelse af katalysatorer og katalytiske processer, og udviklingen af nye og bedre katalysatorer er derfor ofte en tidskrævende og omkostningsfuld proces præget af empiri og af ’trial-and-error’.
En af forklaringerne på den manglende mikroskopiske indsigt i katalysatorens virkemåde, skal findes i katalysatorernes komplekse opbygning, se figur 11.
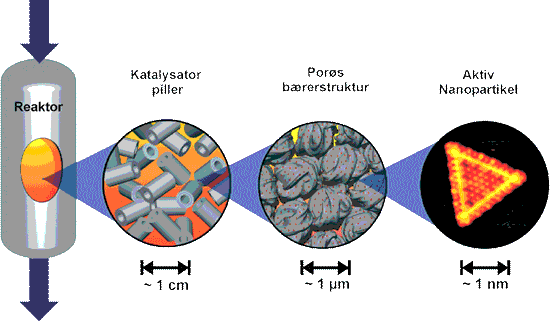
Figur 11
Et kig ind i en reaktor fyldt med en katalysator formet som piller af et porøst bærermateriale,
hvorpå de aktive, få nanometer brede nanopartikler sidder.
En typisk såkaldt heterogen katalysator består af meget små aktive nanopartikler med en diameter på 10–100 nm, der sidder fordelt på overfladen af et bæremateriale med et meget stort overfladeareal. På den måde skabes der en enorm kontaktflade mellem de aktive partikler og reagerende gasser eller væsker.
Et gram af en katalysator kan have et areal i størrelsesordenen af flere parcelhusgrunde! Reaktionsbetingelserne komplicerer tingene endnu mere, idet katalytiske processer typisk foregår ved en høj temperatur og ofte også ved et tryk på mange atmosfære.
Forskningen i nanoteknologi er nu begyndt at ændre måden, som nye katalysatorer udvikles på, bl.a. baseret på viden skabt ved iNANO, Aarhus Universitet.
En forudsætning for at kunne skræddersy en ny katalysator er evnen til at styre, hvordan reaktanterne først splittes og derefter samles til nye produkter på katalysatorens overflade. Da nanoteknologi netop handler om at kunne kontrollere materialer og molekyler på nanometerskala forventes det, at indsatsen inden for nanovidenskab vil give anledning til en markant hurtigere udvikling af bedre katalysatorer i fremtiden.
Ved iNANO er der blevet opbygget en række unikke faciliteter til studier af katalysatorer. Med et hjemmebygget Skanning Tunnel Mikroskop (STM) kan man direkte afbilde, hvordan en katalysator er sammensat – atom for atom – og i nogle tilfælde direkte observere de enkelte trin i de kemiske reaktioner. Dette har givet en unik indsigt i katalysatorers virkemåde, specielt i den atomare struktur af den katalysator, der bruges til at fjerne svovl fra råolie, se boks.
Løsningen på mange aktuelle energi- og miljømæssige problemstillinger afhænger i høj grad af, om det lykkes at udvikle bedre katalysatorer. Konkrete anvendelser til bl.a. reduktion af forureningen fra biler og kraftværker samt udviklingen af alternativer til benzin og diesel som brændstof til transport kræver en markant forøgelse af en række katalysatorers effektivitet.
Studiet af afsvovlingskatalysatoren er et eksempel på, hvordan de redskaber og den viden, der skabes inden for nanoteknologien direkte kan anvendes til at studere modelsystemer for en kompleks katalysator.
Det er lykkedes for den danske katalysatorproducent Haldor Topsøe A/S at videreudvikle afsvovlingskatalysatoren direkte på baggrund af den detaljerede indsigt, der er opnået med STM. Dermed er der skabt en ny generation af mere effektive afsvovlingskatalysatorer, der kan opfylde fremtidens miljøkrav.
Myndighederne i EU og USA har for nylig besluttet at reducere miljøbelastningen fra afbrænding af restsvovl i diesel. Råolie indeholder en lang række urenheder, som af praktiske såvel som miljømæssige hensyn skal fjernes, før olien raffineres til benzin, diesel og andre olieprodukter. Specielt har indholdet af svovl i råolie fået meget opmærksomhed, idet afbrændingen af olieprodukter med svovl i sidste ende giver anledning til syreregn, forsuring af vandløb og søer og udbredt skovdød.
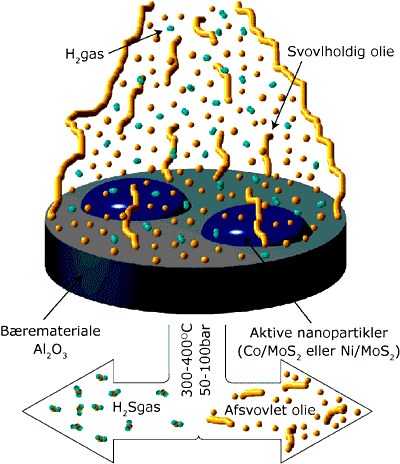 |
Figur 12
En skitse af afsvovlingsprocessen. Det svovlholdige olie ledes sammen med brint igennem katalysatoren ved højt tryk og temperatur, hvorved svovl fjernes som svovlbrinte. |
Svovl kan fjernes katalytisk ved en proces, der hedder afsvovling, se figur 12. Desværre er de nuværende katalysatorer ganske enkelt ikke effektive nok til at reducere svovlindholdet. Lovgivningen i EU kræver, at svovlindholdet i diesel skal reduceres fra de nuværende 350 ppm (parts-per-million) til 50 ppm inden år 2005. I Californien, hvor miljølovgivningen er blandt de skrappeste i verden, skal det ned på 10 ppm, så behovet og interessen for mere effektive katalysatorer er markant og påtrængende.
Det overordnede princip bag afsvovlingskatalysatorens virkemåde har været kendt i årevis, men det har indtil nu ikke været muligt at iagttage katalysatoren på atomart niveau, og der resterer derfor en række fundamentale spørgsmål.
- Hvad er fx den detaljerede form af nanopartiklerne i katalysatoren?´
- Hvordan sidder atomerne i specielt kantområderne af nanopartiklerne i forhold til hinanden?
- Hvor sidder de katalytisk aktive centre?
Alt dette er aldrig før blevet observeret direkte på en atomar skala, men Skanning Tunnel Mikroskopet (STM) har ændret ved dette.
Ved iNANO er det lykkedes at skabe en realistisk model af katalysatoren i laboratoriet og på kontrolleret vis studere dens atomare opbygning og katalytiske aktivitet med STM. De aktive nanopartikler i afsvovlingskatalysatoren består hovedsageligt af molybdændisulfid (MoS2). Ved at fordampe metallisk molybdæn på en guldoverflade under tilførsel af svovlbrinte (H2S) lykkedes det at danne MoS2 nanopartikler med en karakteristik og størrelse lig nanopartiklerne i afsvovlingskatalysatoren.
Figur 13 viser et atomart opløst STM billede af en ca. 3 nm bred MoS2 nanopartikel. STM billederne af de trekantede nanopartikler afslører adskillige overraskelser, bl.a. at MoS2-nanopartiklerne antager en trekantet form i stedet for en sekskant, som man ville forvente fra krystalstrukturen af MoS2. Denne viden har stor indflydelse på forståelsen af katalysatorens virkemåde. Kun kanterne af partiklen er reaktive, og kanterne på en trekantet og en sekskantet partikel er strukturelt forskellige.
Katalysatoren er dog, som den er vist i figur 13, ikke katalytisk aktiv endnu. Den skal først aktiveres ved, at brintmolekyler ledes hen over den. Herved bliver der dannet svovlbrinte (H2S) og der bliver efterladt en tom plads, en såkaldt svovlvakance, som man mener er det aktive center i katalysatoren.
 |
 |
| Figur 13
Skanning Tunnel Mikroskopi billede af en trekantet MoS2 nanopartikel. Billedet viser strukturen af katalysatorpartiklen atom for atom. |
Figur 14
Et STM billede af en tilsvarende trekantet MoS2 nanopartikel, der er blevet aktiveret med brint. Læg mærke til, at nu mangler der svovlatomer på kanten af partiklen. |
Det aktive center vil kunne binde svovl fra et oliemolekyle, som “svømmer” forbi. Derved fjernes svovl fra råolien og bindes til katalysatorpartiklen. Svovlet på partiklen kan så reagere med et nyt brintmolekyle og danne en ny vakance, hvilket slutter den katalytiske cyklus.
Figur 14 viser et STM-billede af en MoS2-trekant i den aktive tilstand. Efter reaktion med små mængder brint ses tydeligt, at enkelte af svovlatomerne mangler langs kanten, hvilket er et direkte bevis for dannelsen af aktive svovlvakancer. Disse nye STM resultater giver et håndgribeligt bevis for princippet bag katalysatorens virkemåde.
Yderligere forskning har vist, at den klare gule rand, der ses langs kanten på de trekantede MoS2 nanopartikler, også spiller en vigtig rolle i afsvovlingsprocessen.
Det er velkendt, at materialer generelt ændrer karakter, når det eksisterer i form af nanopartikler og MoS2 er således ikke en undtagelse. Det viser sig, at den metalliske gule kant vekselvirker overraskende kraftigt med molekylerne i olien, og at det medvirker til at åbne op for strukturen af de ofte meget store og komplekse svovlholdige oliemolekyler. Derved lettes adgangen til svovlatomet, som ofte sidder dybt inde i et aromatisk kulstofmolekyle og svovl kan således lettere reagere med en vakance.